Clay E. Allred e E. Roland Menzel (A Novel Europiumbioconjugate
Method for Latent Fingerprint Detection. In: Forensic
Science International, n.º 85, Elsevier Science Ireland Ltda., 1997, p.
83-94) desenvolveram um novo método de detecção de impressão digital
latente com base em uma reação específica entre o íon európio e lipídios.
A aplicabilidade do método, tanto para superfícies porosas como lisas,
a ausência de solventes clorofluorcarbônicos, a sensibilidade, a rapidez
e o baixo custo são fatores que podem tornar essa abordagem o principal
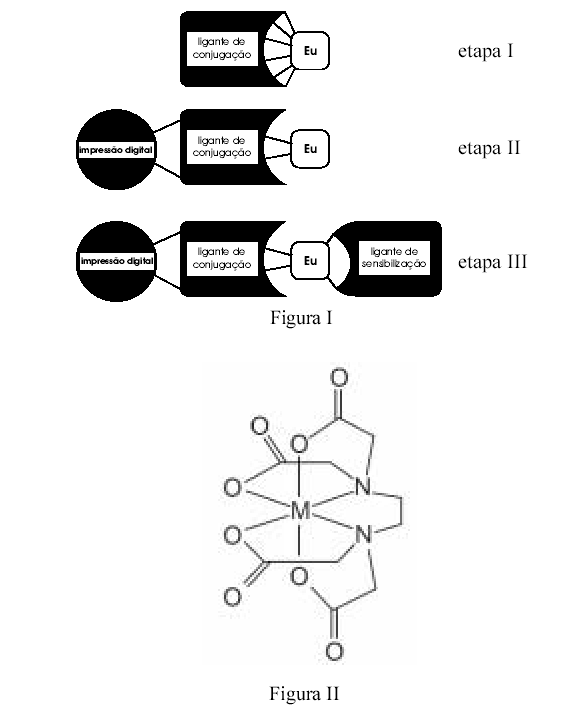
método de detecção de impressão digital em um futuro próximo. Nela,
o ácido etilenodiaminotetracético (EDTA) é usado como ligante de
conjugação que forma um complexo não-fluorescente com o íon európio
(etapa I). Esse complexo é capaz de ligar-se covalentemente a lipídios da
impressão digital (etapa II), na proporção de uma molécula de EDTA-Eu
para cada molécula de lipídio. Nessa reação, algumas ligações entre o íon
európio e o EDTA são desfeitas, expondo parcialmente o íon európio,
que se torna, então, disponível para complexar com outro ligante, como
a 1,10-fenantrolina ou a tenoiltrifluoroacetona (TFA), capaz de
sensibilizar o íon európio a ponto de torná-lo fluorescente (etapa III).
Após esse tratamento, a impressão digital torna-se nitidamente visível
sob excitação por radiação ultravioleta. A figura I acima mostra o
esquema dessas reações e a figura II mostra a estrutura de um complexo
metal-EDTA genérico, em que a letra M representa o íon metálico.
Sendo o EDTA um ácido, é correto afirmar que as
suas soluções aquosas contêm, como cátion, apenas
os íons H3O+, reagem com bases formando sais e
água, são incolores na presença de fenolftaleína,
fazem o papel de tornassol azul ficar vermelho,
conduzem corrente elétrica, são capazes de corroer
metais e possuem sabor azedo.
suas soluções aquosas contêm, como cátion, apenas
os íons H3O+, reagem com bases formando sais e
água, são incolores na presença de fenolftaleína,
fazem o papel de tornassol azul ficar vermelho,
conduzem corrente elétrica, são capazes de corroer
metais e possuem sabor azedo.